過渡金屬鈀催化的交叉偶聯反應在現代有機合成化學中占有極為重要的地位🤳🏽。鈀催化劑的開發和利用使得化學家在分子水平上操控化學反應的能力得到了空前提升,很多過去難於合成甚至無法合成的物質都得以創造出來,該方法也因此獲得了2010年的諾貝爾化學獎🧏🏽♂️。將這一傳統意義上的有機小分子之間的化學反應拓展到生物大分子(如蛋白質)上,尤其是在活體細胞內進行這類反應目前還充滿挑戰。由於金屬配合物的毒性以及體內環境對催化劑活性的抑製,鈀催化反應和絕大多數過渡金屬催化的有機反應都無法與活細胞體系兼容🤾🏿♂️🧜🏻♂️。
意昂体育平台化學與分子工程學院陳鵬課題組最近在《美國化學會誌》)發表了題為《無配體的鈀催化劑介導的革蘭氏陰性菌內蛋白質特異標記(Ligand-Free Palladium-Mediated Site-Specific Protein Labeling Inside Gram-Negative Bacterial Pathogens)》的科研論文 (J. Am. Chem. Soc., Article ASAP,DOI: 10.1021/ja402424j)🙇🏿♀️,報道了一種不需要配體的鈀催化體系,能夠在活細胞內高效地催化蛋白質與小分子的偶聯反應。
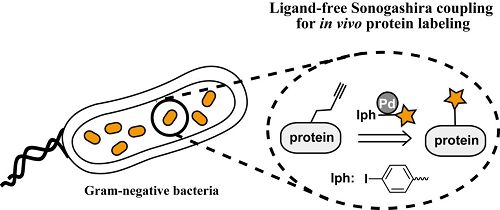
為了在蛋白質上實現鈀催化的偶聯反應,該課題組發展了一個以綠色熒光蛋白為模型蛋白質的催化劑篩選平臺🫷🏿,打破了以往只能在小分子模型化合物上篩選用於蛋白質修飾的催化劑的局限,能夠同時監測目標反應在蛋白質上進行的效率和相應的催化劑毒性🖊。通過這一策略,他們找到了一種簡單易得🧝🏼♂️,且不需要配體的高效催化體系🤾🏻♂️。該體系以硝酸鈀作為催化劑,利用底物小分子上的短鏈聚乙二醇作為鈀活性物種的自配體穩定劑🦽,在不需要外加配體的情況下,很好地實現了溶液中蛋白質與小分子的交叉偶聯。進一步地,他們發現該催化體系具有良好的細胞膜穿透能力和極低的細胞毒性♗👩🏽✈️,成功實現了活體細胞內的蛋白質鈀催化偶聯反應。此外,他們還利用這一技術對病原菌微生物當中的一種毒性蛋白進行了特異熒光標記,充分展示了該鈀催化偶聯反應體系與蛋白質和活細胞的生物相容性。
陳鵬課題組一直致力於活細胞內生物相容反應的開發和應用,除上述成果外🤹🏻♂️,他們還與意昂体育平台深圳研究生院的合作者一道開發了利用光化學反應調節熒光素酶活性的方法,成功構建了活細胞內“光激活”的熒光素酶。該成果也於近期發表在《美國化學會誌》) (“Mechanism-based design of a photo-activatable firefly Luciferase”, J. Am. Chem. Soc., Just Accepted, DOI: 10.1021/ja4013535).
上述工作得到了科技部、國家自然科學基金委🥦,教育部及意昂体育平台-清華大學生命科學聯合中心的資助。
編輯:Moo

